中医药是我国优良传统文化和科学研究的瑰宝,凭借其特有的药效在医学界中独树一帜。目前的研究表明,中药单体甘草酸(GA)具有抑制细胞增殖、促进细胞凋亡、抑制肿瘤血管生成以及肿瘤免疫调节等广泛的抗肿瘤活性。但由于其存在着递送困难、靶向性差以及机体吸收率低等特性,其难以直接应用于临床治疗。为了克服中药单体递送至肿瘤部位的技术壁垒,南京中医药大学韩欣教授团队构建了一种基于肿瘤微环境响应性的基因治疗-纳米中药治疗平台,相关研究成果“DNAzyme-assisted nano-herb delivery system for multiple tumor immune activation”发表于国际知名学术期刊Small(中科院工程技术一区,IF:15.153)上。
脱氧核酶(Deoxyribozyme, DNAzyme)已被报道用于催化RNA/DNA的切割、连接、磷酸化等诸多反应,RNA切割活性的DNAzyme的启动一般需要金属阳离子的激活,如Mn2+、Mg2+和Zn2+等,可用于肿瘤的基因治疗。同时,DNAzyme简单的结构可以较为便捷地实现FAM或Ce6的功能化修饰。而基于免疫检查点阻断(ICB)的肿瘤免疫治疗是基于抑制肿瘤介导的抗癌免疫应答抑制,而不是直接对肿瘤产生毒性的治疗策略。目前研究较多的ICB为PD-1–PD-L1和CTLA4–CD80/CD86,且已成为成熟的肿瘤免疫治疗靶点,PD-L1作为一种I型跨膜蛋白且在大多数肿瘤中高表达,其通过与PD-1结合抑制T细胞增殖和激活以及细胞因子释放等导致免疫抑制。因此,通过基因治疗工具DNAzyme干扰肿瘤细胞PD-L1 mRNA的表达可以有效减缓可能的免疫逃逸的产生。
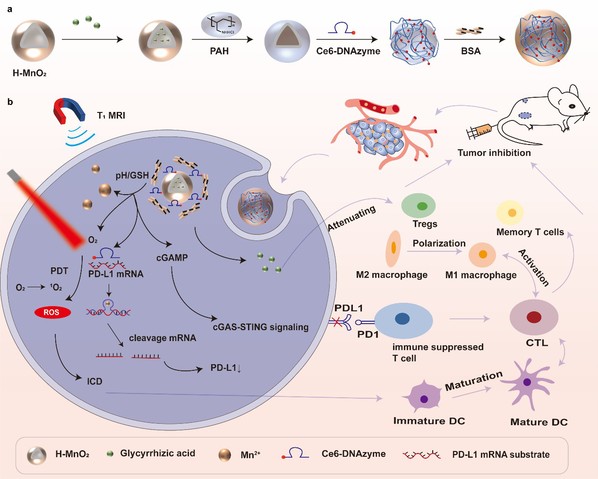
通过构建二氧化锰纳米载体,使得中药单体GA和基因治疗工具Ce6-DNAzyme的靶向递送成为可能。这种pH/谷胱甘肽响应负载GA和Ce6-DNAzyme的二氧化锰纳米平台可用于联合基因治疗和免疫治疗。MnO2纳米粒子可高效递送脱氧核酶和甘草酸,增强肿瘤靶向效应。在肿瘤微环境中,MnO2的生物降解促进了GA和Ce6-DNAzyme在肿瘤部位的释放,光敏剂Ce6和GA可产生活性氧促进免疫原性细胞死亡(ICD),而 Mn2+的产生催化DNAzyme切割活性的同时还可作为cGAS-STING通路的激活剂,实现多重免疫的疗效,相关免疫因子的检测也显示出了其免疫调节的巨大潜能。
硕士研究生杜诗宇为该论文的第一作者,韩欣教授为通讯作者,南京中医药大学为第一通讯单位,该项研究获得国家自然科学基金 (81920108029和31901010)、江苏省社会发展重点基金项目(BE2021741)、江苏省特聘教授自然科学类资助人才项目、江苏省高校优势学科建设工程资助项目(中西医结合) 、江苏省“双创计划”团队项目等资助。
原文链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/smll.202203942
韩欣教授课题组主要从事基于基因编辑技术、微流控芯片技术和功能化生物材料的恶性肿瘤靶标发现和干预研究,近2年相关成果以通讯作者发表在Angewandte Chemie, Small (3篇), Biomaterials, Acta Pharmaceutica Sinica B(2篇), Advanced Healthcare Materials, Biosensors and Bioelectronics, Journal of Experimental & Clinical Cancer Research等国内外主流学术论文12篇(10篇IF>10且中科院1区),其中3篇杂志封面或封底文章。(撰稿人:韩欣 审核人:韩欣 关晓伟)
